국내 코로나바이러스감염증-19 치료제 및 백신 개발에 대한 기대치가 높아지고 있는 가운데 코로나19 바이러스를 중화(무력화)해 만든 치료제가 임상 마지막 단계인 3상에 진입할수 있게돼 기대감을 높이고 있다.
식품의약품안전처(이의경 처장)는 국내 개발 코로나19 중화항체치료제 ‘CT-P59’에 대하여 2/3상 임상시험을 9월 17일 승인했다고 밝혔다.
이번에 승인한 ‘CT-P59’는 셀트리온에서 신약으로 개발 중인 유전자재조합 중화항체치료제이다. 치료원리는 코로나19 바이러스의 표면에 있는 인체 세포와 결합하는 부위에 항체치료제가 대신 붙음으로써 감염을 막게 된다.
이로써 현재 국내에서 코로나19 관련하여 임상시험이 진행 중인 치료제 및 백신은 총 19건(치료제 17건, 백신 2건)으로 늘어났다.
-국내 코로나19 임상시험 승인 현황(2020.9.17 기준)
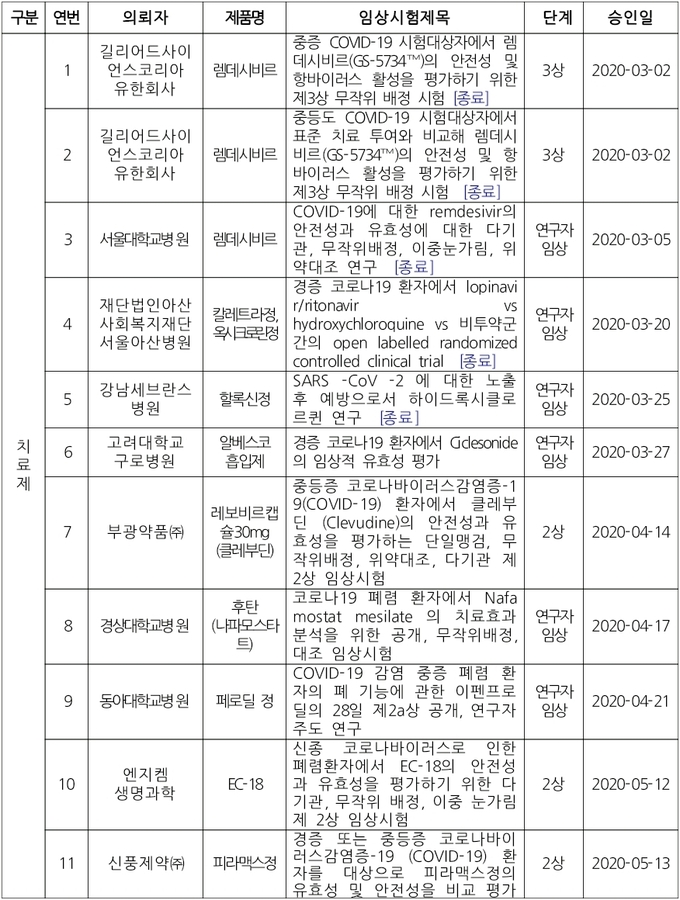
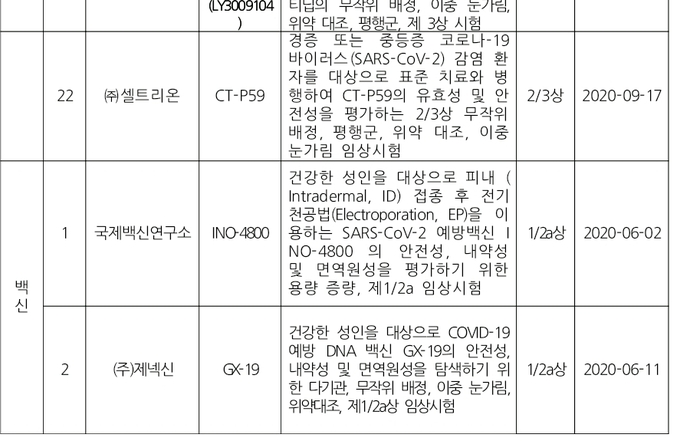
2/3상 임상시험을 동시에 승인받은 CT-P59는 지난 7월과 8월에 승인받은 1상 임상시험의 후속 임상시험으로, 경증부터 중등도 코로나19 환자를 대상으로 유효성과 안전성을 검증하게 된다.
승인과 관련 식약처는 건강한 사람을 대상으로 한 1상 임상시험 결과, CT-P59 투여에 따른 안전성과 내약성*이 확인되어 다음 단계의 임상시험을 진행하는 것이 가능하다고 판단하였다.
특히, 이번 임상시험은 2상과 3상을 동시에 승인한 것으로 2상에서 300명을 대상으로 코로나19 치료를 위한 적절한 투여 용량과 치료효과를 탐색하고, 확인된 용량을 바탕으로 유효성과 안전성 확증을 위한 3상 임상시험을 720명을 대상으로 연속해서 진행하게 된다.
한편 ‘CT-P59’는 미국, 루마니아 등 5개국에도 동시에 임상시험계획을 신청 중이다.
또한, 국외에서도 미국 L社와 R社가 코로나19 중화항체치료제를 개발하여 환자를 대상으로 한 임상시험을 진행하고 있다.
