식품의약품안전처(처장 이의경)는 6월 25일 열린 ‘국제의료기기규제당국자포럼(IMDRF)’ 운영위원회에서 회원국 만장일치로 ‘인공지능 의료기기 국제규제 실무그룹(Artificial Intelligence Medical Devices, AIMDs)’의 초대 의장으로 식약처가 선출되었다고 밝혔다.
이번에 신설된 이 실무그룹은 식약처 주도로 인공지능 의료기기의 정의‧적용대상 등 각종 국제 가이드라인을 제정할 계획이다.
식약처는 그동안 인공지능 의료기기 개발을 지원하고 선도적인 규제환경을 조성하기 위해 다양한 노력을 기울여 왔다.
2017년 세계 최초로 ’인공지능 의료기기 허가·심사 가이드라인‘을 마련하는 등 총 6개의 가이드라인을 발간하여 국내에서 15개사 36개의 인공지능 의료기기를 허가할 수 있는 밑거름이 되었다.
또한, 지난 5월 시행된 「의료기기산업 육성 및 혁신의료기기 지원법」을 제정하여 인공지능 등 혁신의료기기 산업 육성 및 제품 개발 지원을 위한 초석을 마련하였다.
이의경 처장은 “이번 의장 선출은 우리나라 인공지능 의료기기의 규제역량을 국제적으로 인정받은 결과로서, 국내 의료기기 산업의 수출 경쟁력 강화에도 도움이 될 것이다”라고 하였다.
아울러, ”세계보건기구(WHO) 및 국제전기기술위원회(International Electrotechnical Commission, IEC) 등에서도 협력을 주도하여 의료기기 국제 규제조화에 있어서 한국의 역할이 강조될 수 있도록 더욱 노력 하겠다“라고 밝혔다.
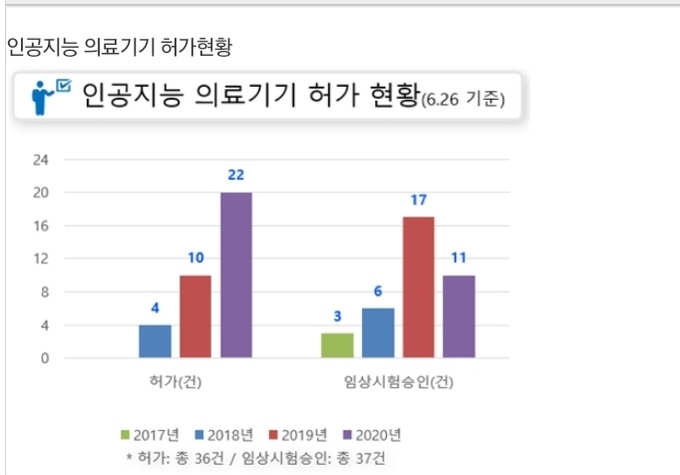
-인공지능 의료기기 허가현황
(‘20.6.26.기준)
업체명 | 제품명(모델명) | 사용목적 | 비고 |
(주)뷰노 | VUNO Med-BoneAge | 골연령 분석 | 기타 |
VUNO Med - Chest X-ray | 흉부 이상부위 검출 보조 | 폐질환 | |
VUNO Med - Fundus AI | 안저 이상부위 진단 보조 | 안과질환 | |
VUNO Med - LungCT AI | 폐결절 검출 보조 | 폐질환 | |
(주)루닛 | Lunit Insight CXR Nodule | 폐결절 검출 보조 | 폐질환 |
Lunit INSIGHT MMG | 유방암 진단 보조 | 유방질환 | |
Lunit INSIGHT CXR MCA | 흉부 이상부위 검출 보조 | 폐질환 | |
㈜클라리파이 | ClariCT.AI | CT 영상의 잡음 제거 및 전송 | 기타 |
㈜딥노이드 | DEEP:SPINE-CF-01 | 요추 압박 골절 의심 부위 검출 보조 | 골절 |
DEEP:CHEST-XR-01 | 흉부 X-Ray 영상 분석 | 기타 | |
DEEP:NEURO-CA-01 | 뇌동맥류 의심 부위 검출 보조 | 뇌질환 | |
㈜제이엘케이 인스펙션 | JBS-01K | 뇌경색 유형 분류 진단 보조 | 뇌질환 |
ATROSCAN | 대뇌 영상 분석 | 뇌질환 | |
JLD-01A | 폐 영상 분석 | 폐질환 | |
JFD-02A | 위 내시경 영상 분석 | 소화계질환 | |
JFD-01A | 대장 내시경 영상 분석 | 소화계질환 | |
JLD-01B | 폐 영상 분석 | 폐질환 | |
JVIEWER-X | 폐 영상 분석 | 폐질환 | |
JOD-01A | 안저 영상 분석 | 안과질환 | |
JSEG-02A | 복부 영상 분석 | 소화계 질환 | |
JBS-04A | 뇌 영상 분석 | 뇌질환 | |
JBS-05A | 뇌 영상 분석 | 뇌질환 | |
JBD-01A | 유방 영상 분석 | 유방질환 | |
삼성전자(주) | Auto Lung Nodule Detection | 폐결절 검출 보조 | 폐질환 |
㈜인피니트헬스케어 | INFINITT Smart Endo | 대장 내시경 영상 분석 | 소화계질환 |
㈜코어라인소프트 | AVIEW | 폐 영상 분석 | 폐질환 |
AVIEW LUNG Nodule CAD | 폐결절 검출 보조 | 폐질환 | |
㈜크레스콤 | MediAI-BA | 골연령 분석 | 기타 |
㈜헬스허브 | Boneage.io | 골연령 분석 | 기타 |
㈜딥바이오 | DeepDx-Prostate | 전립선암 진단 보조 | 전립선 질환 |
㈜이우소프트 | OrthoVision | 치과영상 분석 | 치과질환 |
EzOrtho | 치과영상 분석 | 치과질환 | |
㈜레이언스 | Xmaru Pro BoneAge | 골연령 분석 | 기타 |
Xmaru Pro CXR | 골연령 분석 | 기타 | |
㈜사이넥스 | KardiaMobile System | 부정맥 진단 보조 | 심장질환 |
삼성메디슨(주) | HeartAssist | 태아 심장 초음파 영상 분석 | 심장질환 |
IMDRF 실무그룹 현황 |
* 현재 운영 중인 실무그룹은 8개
|
: 종료 그룹
연번 | 실무그룹명(주도국) | 주요 활동내용 |
1 | 국제 공통허가 심사서류(캐나다) (Regulated Product Submission, RPS) | • 허가를 받기 위해 규제 당국에 제출하는 서류의 공통적인 Template(전자양식 포함)마련을 위한 가이드라인 개발 |
2 | 개인맞춤형 의료기기(호주) (Personalized Medical Devices, PMD) | • 개별 환자를 대상으로 하는 의료기기의 규제를 고려하기 위한 정의 및 규제 절차 가이드라인 개발 |
3 | 체외진단 의료기기 분류 원칙(러시아) (Principles of In Vitro Diagnostic Medical Devices Classification, IVD) | • GHTF의 동일명 문서를 현행화하기 위한 업데이트 작업 계획 중 |
4 | 우수심사기준(미국, 싱가포르) (Good Regulatory Review Practices, GRRP) | • 의료기기 허가 및 GMP 심사자 등 규제 심사자의 자격과 교육 및 역량관리 요구사항을 수립하기 위한 가이드라인 개발 및 단일 허가심사 체계를 목표로 허가 심사 업무 수행하는 기관에 대한 요건 마련 중 |
5 | 이상사례용어(일본) (Adverse Event Terminology, AE) | • IMDRF 의료기기 이상사례용어 및 코드 개발 및 조화를 위한 가이드라인 개발 |
6 | 의료기기 사이버보안(미국, 캐나다) (Medical Device Cybersecurity Guide) | • 의료기기 사이버보안에 대한 규제당국 간 모범사례를 공유하고 이에 대한 국제 공통 사전/사후 규제 마련 |
7 | 의료기기임상평가(중국) (Medical Device Clinical Evaluation, MDCE) | • 규제당국 간 임상평가의 규제조화를 위한 GHTF 가이드라인을 업데이트 |
8 | 인공지능 의료기기(한국) (Artificial Intelligence Medical Devices, AIMDs) | • 의료기기에 적용되는 인공지능 기술인 기계학습 기술을 다루고 기계학습 기술 기반의 의료기기의 주요 공통 용어 개발 |
9 | 기준규격(미국) (Standards) | • 허가‧심사 시 활용되는 의료기기 국제규격 개발에 규제당국자 참여를 위한 활동 및 국가별 표준 활용 분석 |
10 | 의료용 소프트웨어(미국) (Software as a Medical Device, SaMD) | • 의료기기로서 소프트웨어의 용어, 안·유 평가 및 품질관리시스템에 대한 가이드라인의 개발 |
11 | 규제당국간 이상사례 보고체계(유럽연합) (National Competent Authority Report, NCAR) | • 의료기기와 관련된 시판 후 이상사례에 관한 정보 등을 신속하게 교환하여 사망 또는 심각한 손상을 방지하기 위한 가이드라인 개발 |
12 | 품질시스템 단일심사 프로그램(캐나다) (Medical Device Single Audit Program, MDSAP) | • 의료기기 품질관리시스템 등에 대한 표준 요구사항을 개발하여 IMDRF 회원국 간 하나의 품질심사 프로그램을 적용하기 위한 가이드라인 개발 |
13 | 환자정보등록시스템(미국) (Patient Registries, PR) | • 의료기기의 효과성‧신뢰성 등을 평가하기 위해 의료현장 데이터와 의료기기 정보를 DB화하고 관련 이슈를 공유하기 위한 가이드라인 개발 |
14 | 의료기기 고유식별코드(유럽연합) (Unique Device Identification, UDI) | • UDI 제도가 국제조화되도록 UDI 표시기준 지침, 기본 이념 및 실제 시행에 대한 가이드라인 개발 |












