수입식품 등의 생산·제조·가공·처리·포장·보관 등을 하는 해외에 소재하는 시설에 대한 일제 점검결과 관리가 허술한 업체가 무더기 적발됐다.우리 국민들이 믿고 먹는 수입 식품에 대한 보다 세심하고 촘촘한 관리가 요구되고 있다.
식약처는 제조단계부터 수입식품의 안전성을 확보하기 위해 수출국 현지 제조업소에 대해 매년 현지실사를 실시해오고 있는데 지난해 현지실사는 통관·유통 단계 부적합 이력, 다소비 제품, 국내외 위해정보 등을 분석해 위해 우려가 높은 제품을 생산하는 해외제조업소를 대상(32개국 450곳)으로 실시됐다.
식약처는 지난해 국가별 코로나19 방역지침을 고려해 현장 방문이 가능한 국가는 현장조사(269곳)를, 입국 제한 등으로 현장방문이 어려운 국가에 대해서는 비대면 조사(181곳)를 실시했다
현장조사는 현지를 방문해 제조·가공 시설 위생·청결관리, 급수시설 관리, 종업원 위생 관리, 제품 검사관리 등 해외제조업소의 전반적인 위생관리 상태를 중점적으로 봤고,비대면 조사는 해외제조업소의 위생관리 상태를 확인할 수 있는 자료를 제출받아 검토한 후 태블릿 등 이동식 영상장비를 활용하여 현장조사와 동일한 점검항목에 대해 원격으로 제조공장을 확인했다고 식약처는 밝혔다.
현지실사 결과, 총 450곳 중 412곳(91.6%)은 적합했으며 위생관리가 미흡(부적합, 개선필요)한 38곳(8.4%)이 적발됐다.
식약처는 적발된 38곳 중 ‘부적합’ 판정된 24곳에 대해 수입중단 조치를 하고, 국내 유통 중인 해당 제조업소의 제품에 대해 수거·검사를 실시했다.
-위생관리 미흡 제조업소 목록
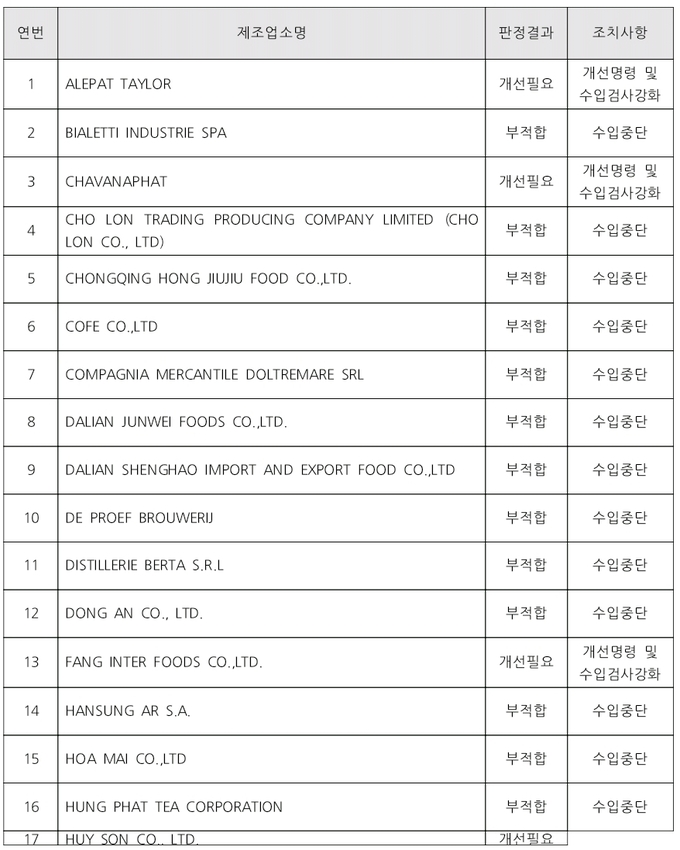
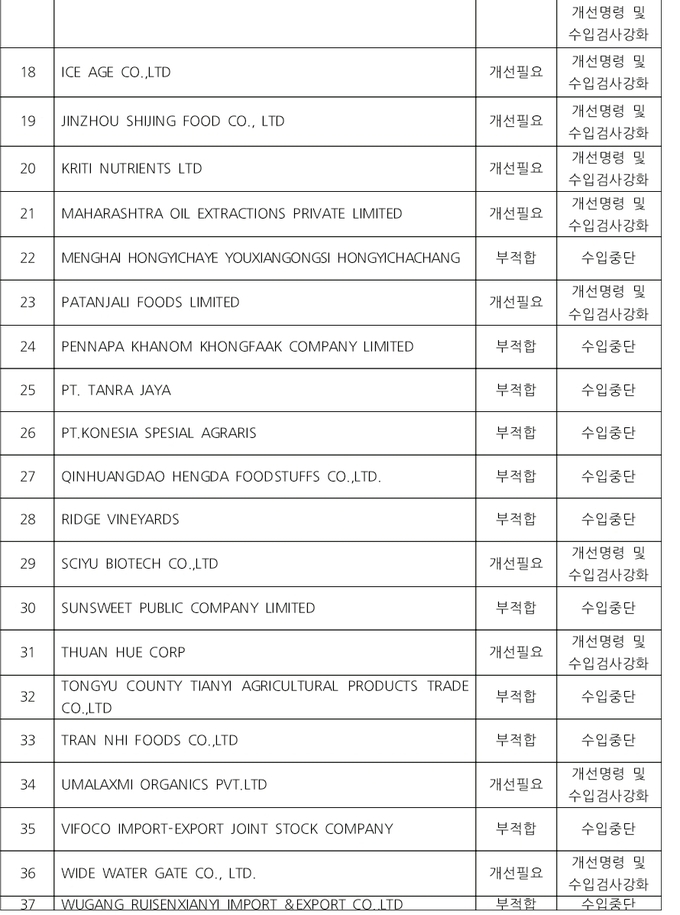
또 ‘개선필요’ 판정된 14곳에 대해서는 개선명령과 수입검사 강화 조치를 하고, 개선 조치가 완료될 때까지 위반 제조업소에서 생산·수입되는 모든 제품에 대해 정밀검사를 실시했다.
특히 향후 위생관리가 미흡한 해외제조업소에서 제출한 개선사항 증빙자료를 검토해 적합한 경우 수입중단 등 조치를 해제할 수 있지만,적발된 업체가 개선사항 증빙자료를 제출하지 않는 경우에는 수입중단 조치가 내려진다.
식품의약품안전처(처장 오유경)는 수입식품에 대한 선제적인 안전관리를 위해 지난해 우리나라로 식품 등을 수출하는 32개 국가 해외제조업소 450곳을 대상으로 현지실사를 실시한 결과, 위생관리가 미흡한 38곳(8.4%)을 적발해 수입중단 등 조치를 통보했다고 27일 밝혔다.
한편 식약처는 작년에 국가별 코로나19 방역지침을 고려해 현장 방문이 가능한 국가는 현장조사(269곳)를, 입국 제한 등으로 현장방문이 어려운 국가에 대해서는 비대면 조사(181곳)를 실시했다.















