질병관리청(청장 지영미) 국립보건연구원(원장직대 장희창)은 코로나19 확진자 다중오믹스 자료, 임상 정보와 인체 자원을 연구목적으로 추가 공개·분양한다고 밝혔다.
국립보건연구원은 코로나19 확진자(300명) 및 일반인(120명) 다중오믹스 분석결과와 임상 정보, 인체 자원을 연구목적으로 2022년 1월 3일 공개·분양한 바 있으며, 생명‧윤리적으로 적법한 동의 절차를 거쳐 코로나19 확진자 459명과 백신 접종자 57명을 포함한 일반인의 임상 정보와 인체 자원을 추가 확보하였다.
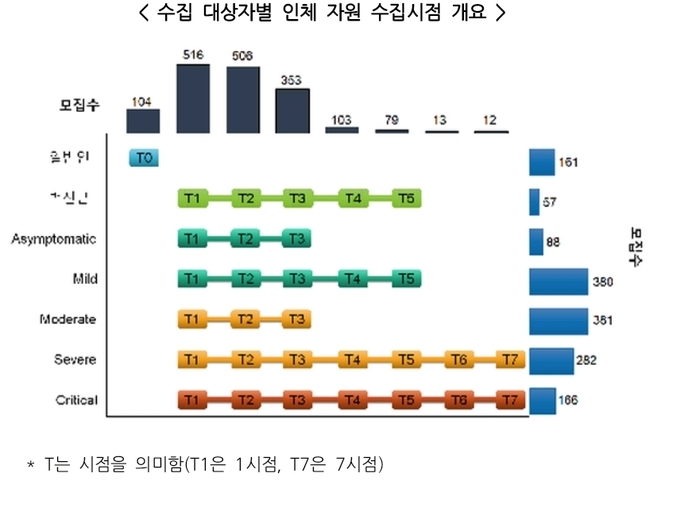
특히, 백신접종자는 백신 접종 전·후 등 5시점의 연구자료가 포함되어 감염에 의한 변화와 비교 분석도 가능하다. 코로나19 확진자 459명은 중증도에 따라서 경증(329, 72%)은 3시점에서, 중증(130명, 28%)은 최대 7시점에서 인체 자원을 추가 확보*하였다.
수집된 인체 자원을 활용하여 질병관리청에서는 일반혈액검사, 191개의 면역 인자(사이토카인) 및 다중오믹스 자료를 추가 생산하였으며 추가 생상된 자료에는 전장유전체분석(WGS), 단일세포 전사체 분석(scRNA-seq), T세포/B세포 수용체 발현정보(bulk TCR/BCR RNAseq) 등 다중오믹스와 인간백혈구항원 유형(HLA typing)을 포함한다.
이렇게 생산된 자료는 코로나19 감염 후 인간의 면역 반응에 심도 있는 분석에 이용되어 중증도 예측, 치료제 개발에 중요한 자료로 활용 가능하다.
국립보건연구원은 후속 사업을 통해서 코로나19 확진자의 단백체 분석 자료를 추가 확보하여 신속하게 공개할 예정이다. 코로나19 확진자 및 일반인 다중오믹스 데이터와 인체 자원은 국립보건연구원 국립중앙인체자원은행을 통해 분양하며, ’23년 3월 27일부터 국립중앙인체자원은행 누리집*에서 신청 접수가 가능하다.신청한 과제는 국립중앙인체자원은행 분양위원회 심의*를 거쳐 연구자에게 제공된다.
















