식품의약품안전처(처장 오유경)는 지난 9월 한 달간 의료제품 총 109개 품목을 허가했다고 밝혔다.올해 9월 의료제품 허가 품목 수는 지난해 월평균(195개) 대비 55.9%, 올해 3분기 월평균(124개) 대비 87.9% 수준이었다.
신약으로는 중증 원형탈모증 치료제인 ‘리트풀로캡슐50밀리그램(리틀레시티닙토실산염)’과 위선암 치료제(CLDN18.2
양성 환자 대상)인 ‘빌로이주100밀리그램(졸베툭시맙)’을 허가하였다. 참고로 ‘빌로이주100밀리그램(졸베툭시맙)’을 안전하고 효과적으로 사용하기 위한 동반 진단의료기기 ‘VENTANA CLDN18 (43-14A) RxDx Assay’도 함께 허가했다.
희귀의약품으로는 B형 혈우병*에 대한 유전자치료제인 ‘헴제닉스주(에트라나코진데자파르보벡)’, 골수섬유증** 치료제인 ‘옴짜라정100밀리그램(모멜로티닙염산염수화물)’등을 허가했다.
- 9월 의료제품 허가 품목 목록
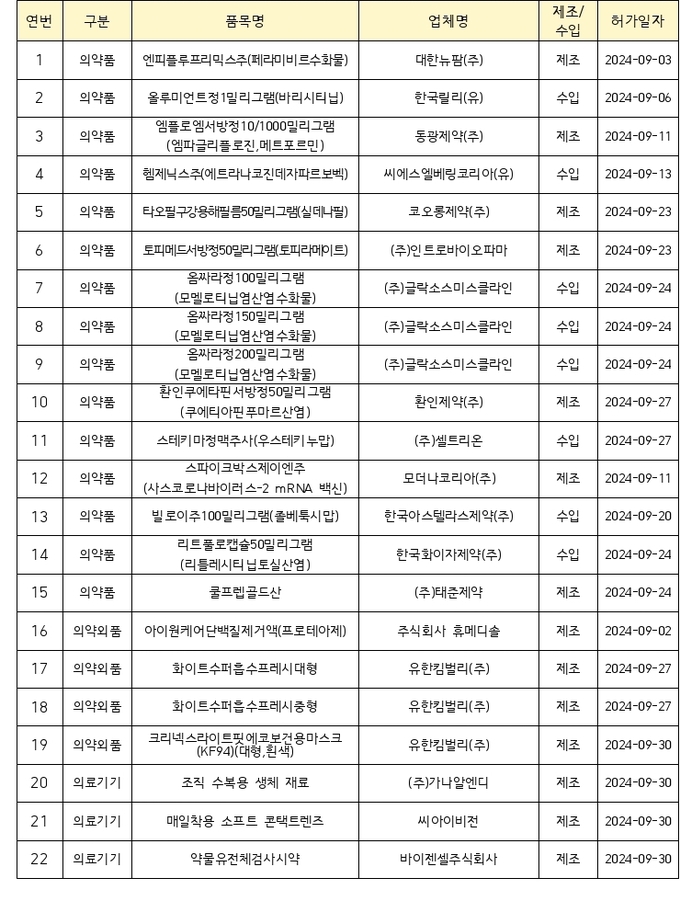

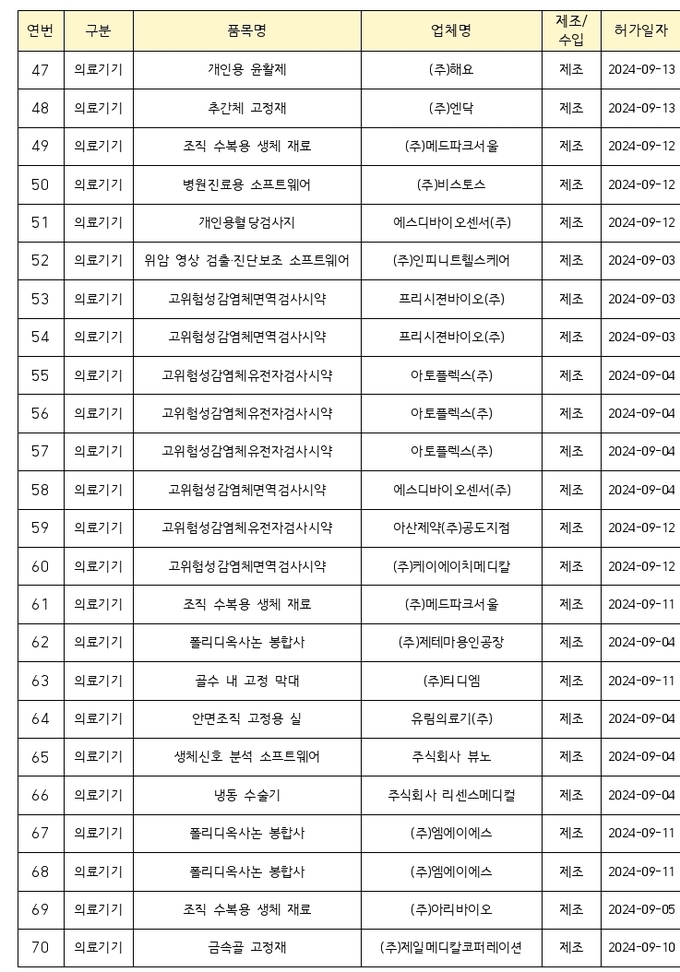
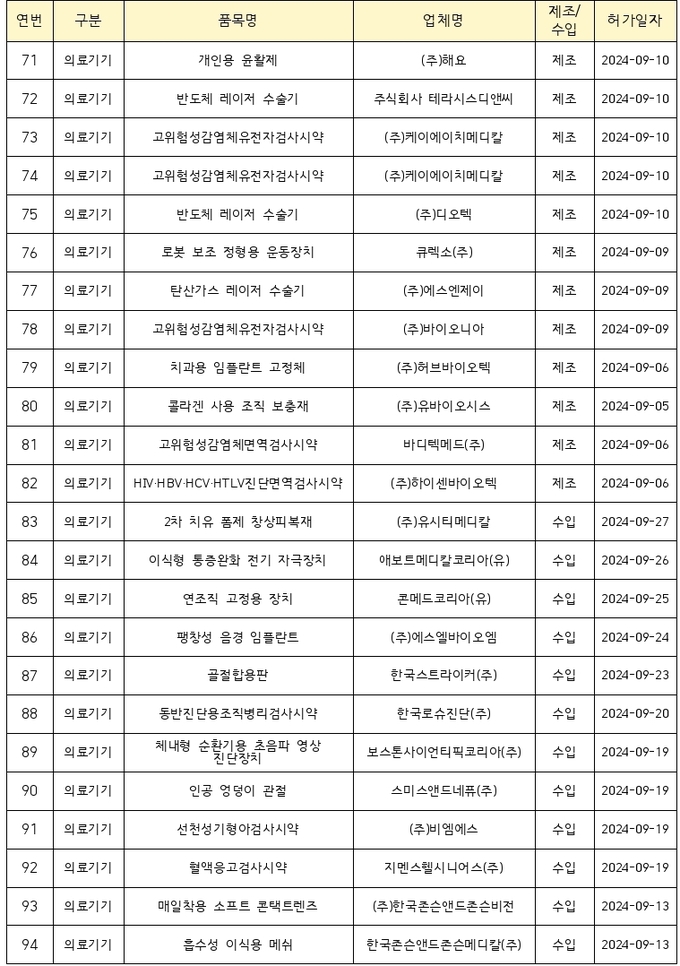
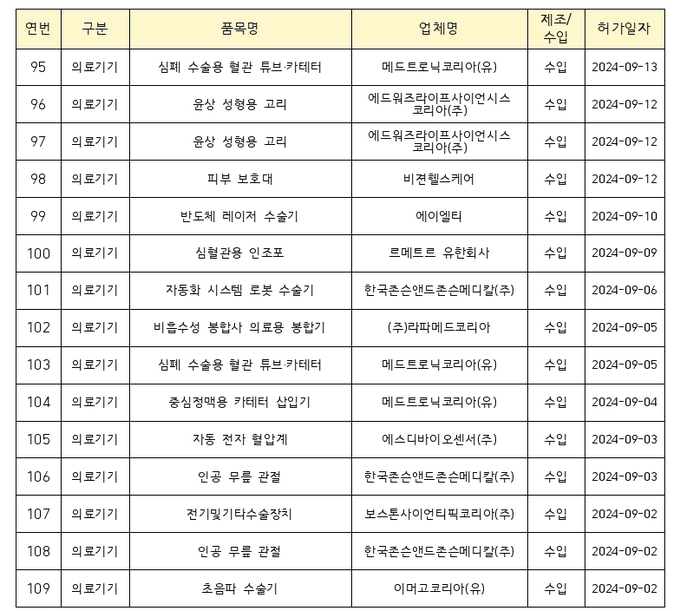
백신은 ’24~’25 절기 예방접종용 코로나19 백신 ‘스파이크박스제이엔주(사스코로나바이러스-2 mRNA 백신)’를 허가했다.
의료기기는 인공지능을 기반으로 소아·청소년 환자의 문진 내용 및 생체지표 검사 결과를 분석하여 폐렴을 포함한 하기도감염의 위험도(확률)를 표시해 주는 소프트웨어 ‘Pneumo-AID for children’를 국내 최초로 허가했다.
















