지난해 신약 ,자료제출의약품 ,안전성·유효성 심사대상 의약외품으로 허가 받은 품목은 모두 2백65개 제품으로 집계됐다. 이 가운데 자료제출의약품이 144개로 가장많았으며,희귀 약품포함한 신약이 81개 품목으로 뒤를 이었다. 안전성 유효성 심사대상 더품은 40개로 나타났다.
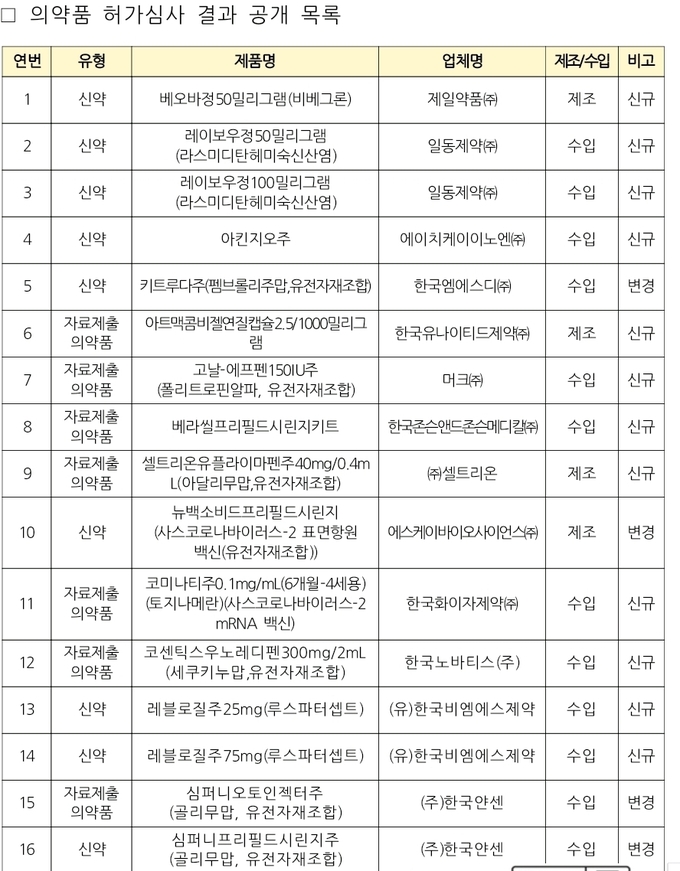

식품의약품안전처(처장 오유경)는 3일 이같은 내용을 담아 의약품과 의약외품 허가심사에 대한 투명성, 일관성, 신뢰성을 강화하기 위해 지난 12월에 의약품 16개, 의약외품 3개 총 19개 품목(신규허가 14개, 변경허가 5개)의 허가심사 결과(허가보고서)와 지난 해 누적 현황을 공개했다.
12월에 허가 받은 대표적인 의약품은 ▲과민성 방광 증상 치료 신약 ‘베오바정50밀리그램’(제일약품㈜) ▲항암 화학요법제 투여에 따른 구역·구토 예방 신약인 ‘아킨지오주’(에이치케이이노엔㈜) ▲편두통에 대한 급성 치료 신약 ‘레이보우정50밀리그램/100밀리그램(라스미디탄헤미숙신산염)’(일동제약㈜) ▲빈혈 치료 신약 ‘레블로질주25mg/75mg(루스파터셉트)’((유)한국비엠에스제약)가 있다.













